เนื้อหา
ปฏิกิริยาเคมีบางอย่างเรียกว่าปฏิกิริยาย้อนกลับได้เพราะสามารถไปได้สองทิศทาง: ไปข้างหน้าและย้อนกลับ ปฏิกิริยาเหล่านี้เกิดขึ้นพร้อมกันและไม่เคยหยุดนิ่งดังนั้นจึงเรียกว่าปฏิกิริยาแบบไดนามิก ปฏิกิริยาอยู่ในภาวะสมดุลเมื่ออัตราของปฏิกิริยาทั้งสองเท่ากัน อย่างไรก็ตามในขณะที่ความเข้มข้นของสารตั้งต้นและผลิตภัณฑ์มีค่าคงที่พวกเขาไม่จำเป็นต้องเท่ากัน ค่าคงที่สมดุลบางครั้งเรียกว่าค่า keq หากคุณกำลังทดลองกับปฏิกิริยากรดเบสค่า keq คือ ลำลูกกาหรือที่เรียกว่าค่าคงที่ความเป็นกรดซึ่งวัดความแข็งแรงของกรดในสารละลาย
TL; DR (ยาวเกินไปไม่ได้อ่าน)
ในปฏิกิริยากรด - เบสค่าคงที่สมดุล (ค่า keq) เป็นที่รู้จักกัน ลำลูกกา. ในการออกกำลังกาย Ka เมื่อคุณรู้จัก pKa ใช้เครื่องคิดเลขเพื่อค้นหา antilog
ค่า pKa
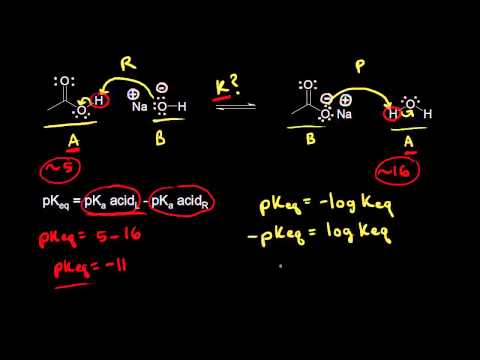
เมื่อกรดแตกตัวในน้ำมันจะปล่อยโปรตอนออกมาเพื่อทำให้สารละลายนั้นเป็นกรด อย่างไรก็ตามมีเพียงกรดอ่อน ๆ ที่แยกตัวออกจากน้ำได้เพียงบางส่วนเท่านั้นที่มีทั้งสถานะที่แยกตัวออกจากกัน (A-) และสถานะที่ไม่เกี่ยวข้อง (AH) พวกมันอยู่ด้วยกันตามสมการสมดุล AH ⇌ A- + H +. อัตราส่วนความเข้มข้นของทั้งสองด้านเป็นค่าคงที่โดยมีเงื่อนไขการวิเคราะห์คงที่ นี้เป็น ลำลูกกาซึ่งถูกกำหนดโดยสมการ Ka = ÷ ที่เครื่องหมายวงเล็บแสดงความเข้มข้นของส่วนประกอบสัมพัทธ์ เนื่องจากค่าคงที่ของ Ka สำหรับกรดอาจเป็นจำนวนที่ยาว (ตัวอย่างเช่น Ka สำหรับกรดอะซิติกคือ 0.000018) จึงไม่สะดวกในการแสดงความเป็นกรดโดยใช้ค่าคงที่ของ Ka เพียงอย่างเดียว ค่า pKa ถูกนำมาใช้เป็นดัชนีเพื่ออธิบายความเป็นกรดของกรดอ่อนที่กำหนดเป็น pKa = -log Ka.
การค้นหา Keq จาก pKa
หากคุณมีค่า pKa ของสารประกอบอยู่แล้วคุณสามารถหาค่า Ka ของมันได้ ตัวอย่างเช่นค่า pKa ของกรดแลคติคคือ 3.86 สิ่งแรกที่คุณทำคือคูณค่า pKa ด้วยค่าลบเพื่อกลับเข้าสู่ระบบ ในกรณีของกรดแลกติกนี่คือ 3.86 x (-1) = -3.86 จากนั้นใช้เครื่องคิดเลขเพื่อเพิ่ม 10 ให้กับพลังของ pKa เชิงลบ ในทางคณิตศาสตร์สิ่งนี้เรียกว่า antilog และโดยปกติกุญแจจะมีเครื่องหมาย 10x เกี่ยวกับเครื่องคิดเลขวิทยาศาสตร์ ซึ่งหมายความว่า Ka ของกรดแลคติกคือ 10(-3.86)ซึ่งคือ 1.38 x 10-4 หรือ 0.000138 ยิ่งค่า pKa เล็กลงเท่าใดกรดก็จะยิ่งรุนแรงขึ้น นี่หมายถึงกรดแลคติคที่มีค่า pKa 3.86 เป็นกรดที่แข็งแกร่งกว่ากรดอะซิติกซึ่งมีค่า pKa เท่ากับ 4.75