เนื้อหา
สารประกอบที่นำกระแสจะถูกยึดเข้าด้วยกันโดยแรงไฟฟ้าสถิตหรือแรงดึงดูด ประกอบด้วยอะตอมหรือโมเลกุลที่มีประจุบวกเรียกว่าไอออนบวกและอะตอมหรือโมเลกุลที่มีประจุลบเรียกว่าประจุลบ ในสถานะที่เป็นของแข็งสารประกอบเหล่านี้จะไม่นำไฟฟ้า แต่เมื่อละลายในน้ำไอออนจะแยกตัวและสามารถทำกระแสได้ ที่อุณหภูมิสูงเมื่อสารประกอบเหล่านี้กลายเป็นของเหลวแคทไอออนและแอนไอออนเริ่มไหลและสามารถนำกระแสไฟฟ้าได้แม้ในกรณีที่ไม่มีน้ำ สารประกอบที่ไม่ใช่อิออนหรือสารประกอบที่ไม่แยกตัวออกเป็นไอออนจะไม่เกิดกระแสไฟฟ้า คุณสามารถสร้างวงจรอย่างง่ายโดยใช้หลอดไฟเป็นตัวบ่งชี้เพื่อทดสอบค่าการนำไฟฟ้าของสารประกอบน้ำ สารประกอบทดสอบในการตั้งค่านี้จะทำให้วงจรเสร็จสมบูรณ์และเปิดหลอดไฟหากสามารถทำกระแสได้
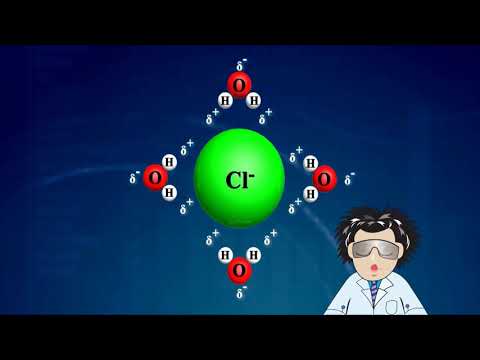
สารประกอบที่มีความนำไฟฟ้าสูง
วิธีที่ง่ายที่สุดในการตรวจสอบว่าสารประกอบสามารถดำเนินการในปัจจุบันคือการระบุโครงสร้างโมเลกุลหรือองค์ประกอบของมัน สารประกอบที่มีค่าการนำไฟฟ้าสูงจะแยกตัวออกเป็นอะตอมหรือโมเลกุลที่มีประจุหรือไอออนที่มีประจุเมื่อละลายในน้ำ ไอออนเหล่านี้สามารถเคลื่อนย้ายและพกพากระแสได้อย่างมีประสิทธิภาพ ยิ่งความเข้มข้นของไอออนสูงขึ้นเท่าใดก็ยิ่งนำไฟฟ้าได้มากเท่านั้น เกลือแกงหรือโซเดียมคลอไรด์เป็นตัวอย่างของสารประกอบที่มีค่าการนำไฟฟ้าสูง มันแยกตัวเป็นโซเดียมที่มีประจุบวกและคลอรีนไอออนที่มีประจุลบในน้ำ แอมโมเนียมซัลเฟต, แคลเซียมคลอไรด์, กรดไฮโดรคลอริก, โซเดียมไฮดรอกไซด์, โซเดียมฟอสเฟตและสังกะสีไนเตรตเป็นตัวอย่างอื่น ๆ ของสารประกอบที่มีการนำความร้อนสูงหรือที่เรียกว่าอิเล็กโทรไลต์ที่แข็งแกร่งอิเล็กโทรไลต์ที่แรงมีแนวโน้มที่จะเป็นสารประกอบอนินทรีย์ซึ่งหมายความว่าพวกมันขาดอะตอมคาร์บอน สารประกอบอินทรีย์หรือสารประกอบที่ประกอบด้วยคาร์บอนมักจะอิเล็กโทรไลต์ที่อ่อนแอหรือไม่เป็นตัวนำไฟฟ้า
สารประกอบที่มีค่าการนำไฟฟ้าต่ำ
สารประกอบที่แยกออกจากกันเพียงบางส่วนในน้ำคืออิเล็กโทรไลต์อ่อนและตัวนำที่ไม่ดีของกระแสไฟฟ้า กรดอะซิติกซึ่งเป็นสารประกอบในน้ำส้มสายชูเป็นอิเล็กโทรไลต์ที่อ่อนตัวเนื่องจากมันจะแยกตัวออกจากน้ำเพียงเล็กน้อยเท่านั้น แอมโมเนียมไฮดรอกไซด์เป็นอีกตัวอย่างหนึ่งของสารประกอบที่มีค่าการนำไฟฟ้าต่ำ เมื่อมีการใช้ตัวทำละลายอื่นนอกเหนือจากน้ำจะทำให้เกิดการแยกตัวของไอออนิกดังนั้นความสามารถในการรับกระแสจึงเปลี่ยนไป ไอออนไนซ์ของอิเล็กโทรไลต์ที่อ่อนแอมักเพิ่มขึ้นตามอุณหภูมิที่เพิ่มขึ้น เพื่อเปรียบเทียบค่าการนำไฟฟ้าของสารประกอบต่าง ๆ ในน้ำนักวิทยาศาสตร์ใช้สื่อกระแสไฟฟ้าเฉพาะ ค่าสื่อกระแสไฟฟ้าที่เฉพาะเจาะจงคือการวัดค่าการนำไฟฟ้าของสารประกอบในน้ำที่อุณหภูมิเฉพาะซึ่งมักจะเป็น 25 องศาเซลเซียส ความเป็นสื่อกระแสไฟฟ้าที่เฉพาะเจาะจงจะถูกวัดเป็นหน่วยของซีเมนส์หรือไมโครไซม์ต่อเซนติเมตร สามารถกำหนดระดับมลพิษทางน้ำโดยการวัดค่าสื่อกระแสไฟฟ้าเฉพาะเนื่องจากน้ำเสียมีไอออนมากขึ้นและสามารถสร้างสื่อกระแสไฟฟ้าได้มากขึ้น
สารประกอบที่ไม่เป็นตัวนำ
สารประกอบที่ไม่ก่อให้เกิดไอออนในน้ำไม่สามารถทำกระแสไฟฟ้าได้ น้ำตาลหรือซูโครสเป็นตัวอย่างของสารประกอบที่ละลายในน้ำ แต่ไม่ได้ผลิตไอออน โมเลกุลของซูโครสที่ละลายในน้ำนั้นล้อมรอบด้วยกลุ่มโมเลกุลของน้ำและถูกกล่าวถึงว่าเป็นไฮเดรท แต่ยังคงไม่มีประจุ สารประกอบที่ไม่ละลายในน้ำเช่นแคลเซียมคาร์บอเนตไม่มีการนำไฟฟ้าพวกมันไม่ก่อให้เกิดไอออน การนำไฟฟ้าต้องการอนุภาคที่มีประจุ
การนำไฟฟ้าของโลหะ
การนำไฟฟ้าต้องการการเคลื่อนที่ของอนุภาคที่มีประจุ ในกรณีของอิเล็กโทรไลต์หรือสารประกอบไอออนิกเหลวหรือหลอมเหลวอนุภาคที่มีประจุบวกและลบจะถูกสร้างขึ้นและสามารถเคลื่อนที่ไปรอบ ๆ ได้ ในโลหะไอออนของโลหะบวกจะถูกจัดเรียงในโครงตาข่ายแข็งหรือผลึกที่ไม่สามารถเคลื่อนที่ได้ แต่อะตอมโลหะที่เป็นบวกนั้นล้อมรอบด้วยกลุ่มเมฆอิเล็กตรอนที่สามารถเคลื่อนที่ไปรอบ ๆ ได้และสามารถส่งกระแสไฟฟ้าได้ การเพิ่มขึ้นของอุณหภูมิทำให้ค่าการนำไฟฟ้าลดลงซึ่งตรงกันข้ามกับการเพิ่มขึ้นของการนำไฟฟ้าโดยอิเล็กโทรไลต์ภายใต้สถานการณ์ที่คล้ายคลึงกัน